在纳米酶驱动的肿瘤治疗领域,精准调控纳米材料的电子态对干预癌细胞内的氧化还原稳态具有决定性意义。稀土元素因其独特的4f轨道电子构型,成为潜在的高效抗肿瘤催化剂。然而,4f电子具有强局域性、显著的屏蔽效应及自旋-轨道耦合特性,导致其电子态难以通过传统方法有效调控,严重制约了其催化活性提升与生物医学应用拓展。
非晶材料因具备“短程有序、长程无序”的结构特征,富含结构缺陷和不饱和配位位点,可增强4f轨道间的轨道重叠与杂化,从而实现对稀土元素电子态的动态调控,提升其催化活性,为开发高效抗肿瘤纳米酶提供了全新思路。
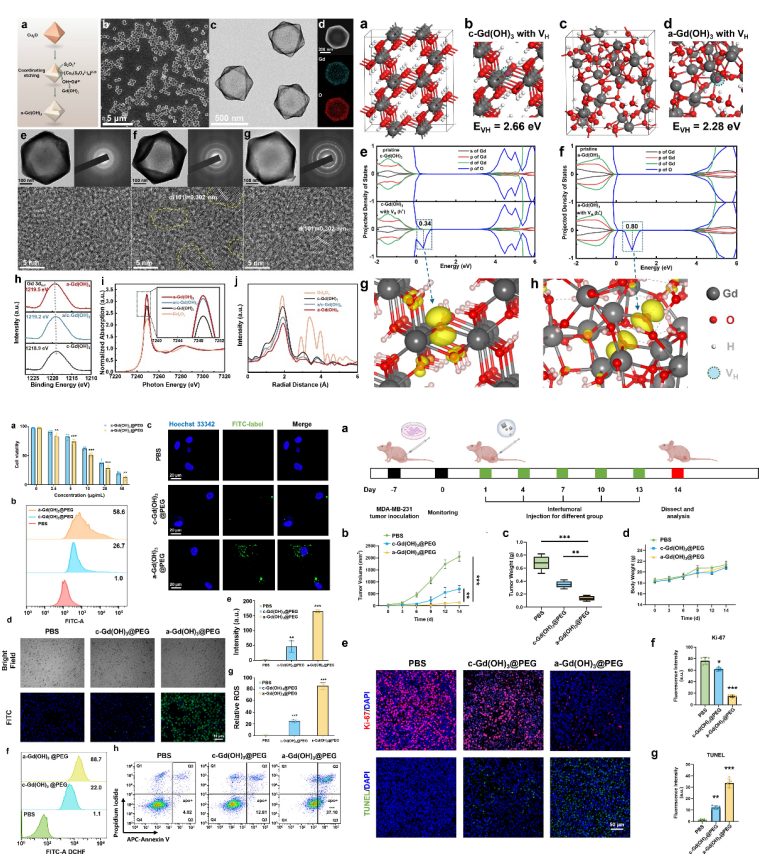
针对以上科学问题,作者基于郭林教授团队于2013年首次提出的“界面限域配位刻蚀”策略(J. Am. Chem. Soc., 2013, 135, 16082),设计并合成了一种非晶笼状Gd(OH)3纳米酶,非晶化显著降低Gd-O配位数并改变4f电子态,增强空穴离域性,使原本惰性的 Gd3+(半满4f7轨道)展现出优异的过氧化物酶(POD)样活性,其Kcat达3.49×10⁴ s-1,高于天然HRP酶的一个数量级。经PEG修饰后,纳米笼在肿瘤微环境(pH ≈ 5.5)中可被特异性激活,通过高效产生活性氧(ROS)抑制肿瘤生长,展现出优异的治疗潜力,为稀土纳米材料在生物医学领域的应用拓展提供了新方向。
Zezhou Wang, Qi Hu, Mengmeng Zhang, Chen Li, Shu Wang, Yanhong Li, Fengshi Li, Tianqi Guo*, Pengfei Hu*, Kewei Jiang*, Gilberto Teobaldi, Li-Min Liu*, and Lin Guo* Amorphization-Induced Electronic Modulation of Gd (OH)3 Nanocages with Enhanced Enzymatic Activities for Antitumor Therapy. Journal of the American Chemical Society 2025.
https://doi.org/10.1021/jacs.5c09591